
数据集概述
本次分析研究了 GSE124647,这是一个转移性乳腺癌基因表达数据集,涉及 140 名患者,在 Affymetrix Human Genome U133 Plus 2.0 芯片(22,283 个探针组)上进行了分析。患者被分为生存良好组(OS > 24.05 个月或数据被删除,n=88)和生存较差组(OS ≤ 24.05 个月且出现死亡事件,n=52)。全面工作流程包括差异表达分析、通路富集和分子分型,以识别与生存相关的标志和治疗漏洞。
最显著基因及其功能
最显著的生存相关基因
差异表达分析确定了 70 个显著与整体生存相关的基因(FDR < 0.05),具有显著的不对称调控模式:41 个基因在生存较差中下调,29 个基因上调。
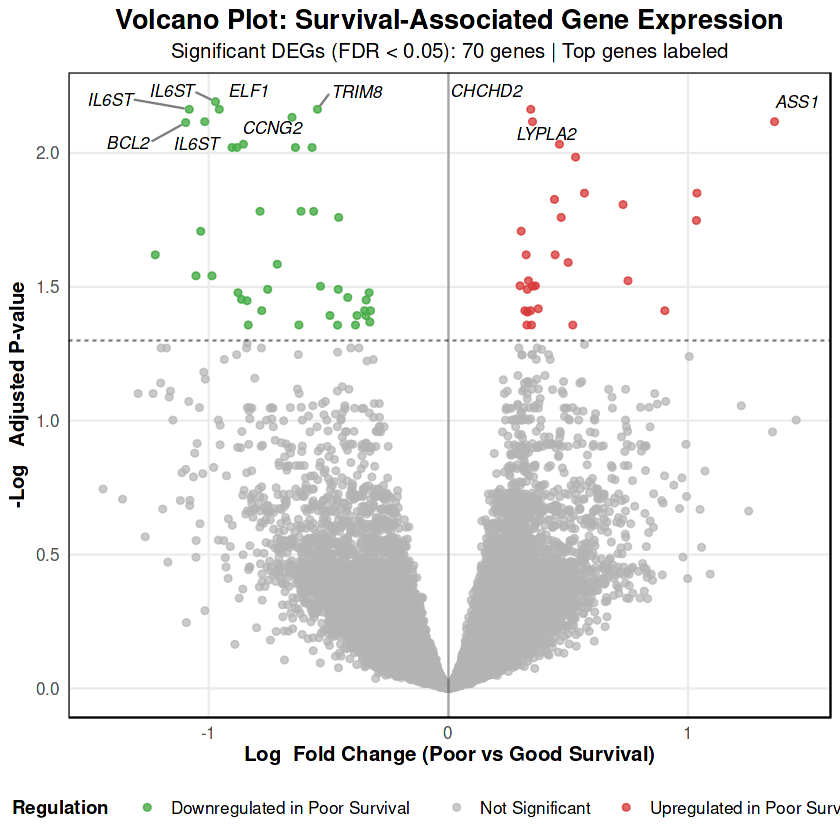
前 6 个基因的表达模式显示出在生存组之间的强大区分能力,基因符号现在可以清晰地识别每个生物标记。
IL6ST(白细胞介素 6 信号转导酶)作为最强的生物标记出现,4 个独立探针组(212196_at, 212195_at, 204864_s_at, 203685_at)全部在生存较差中表现出一致的下调(logFC 范围:-0.97 到 -1.08,所有 FDR < 0.01)。IL6ST 编码 gp130,即整个 IL-6 细胞因子家族的必需共受体,其多探针一致性提供了极高的信心即 受损的 JAK-STAT 信号传导是生存较差的核心特征 在转移性乳腺癌中。
ASS1(精氨酸代琥珀酸合成酶 1)在生存较差中表现出最强的上调(logFC = +1.36,FDR = 7.64×10⁻³)。作为精氨酸生物合成的限速酶,ASS1 提升表明 代谢重编程朝向合成代谢通路,可能支持转移性定殖,但也会产生可以被治疗性利用的精氨酸营养缺乏。
BCL2(BCL2 凋亡调节因子)在生存较差中表现出矛盾的下调(logFC = -0.80)。BCL2 的丧失在这种转移性背景下并不代表肿瘤抑制,而是反映了 增强的凋亡易感性和细胞平衡的丧失,如通路富集显示的 p53 和外源性凋亡信号通路失调所证实。
其他关键基因包括:
CCNG2(细胞周期蛋白 G2, logFC = -0.65):细胞周期检查点破坏
SHMT2(丝氨酸羟甲基转移酶 2, logFC = +0.82):一碳代谢激活
NFIB(核因子 I/B, logFC = +0.75):转录重编程
LARP1(La 相关蛋白 1, logFC = -0.70):RNA 处理功能紊乱
TPI1(磷酸甘油转移酶 1, logFC = +0.68):糖酵解增强
INPP4B(肌醇聚磷酸酯4-磷酸酯酶 II, logFC = +0.65):肿瘤抑制维持
BTN3A3(乳球蛋白 3A3, logFC = -0.60):免疫检查点功能障碍
STAT6(信号转导激活转录因子 6, logFC = -0.58):IL-4/ IL-13 信号损伤
功能基因分类
这70个显著基因聚集为五个主要功能主题:
1. 免疫系统功能障碍(4个基因):IL6ST↓, BTN3A3↓, STAT6↓, ELF1↓ — 代表免疫耗竭通过 JAK-STAT 扰乱、检查点失效和转录抑制
2. 凋亡与细胞死亡(4个基因):BCL2↓, PMAIP1↑, TP53INP1↑, CDKN1A↑ — 表明失调细胞死亡伴随失去抗凋亡保护和增强的p53-介导应激反应
3. 代谢与生物合成(3个基因):ASS1↑, SHMT2↑, TPI1↑ — 反映一致的代谢重编程贯穿精氨酸生物合成、一-碳代谢和糖酵解
4. 增长控制与肿瘤抑制(2个基因):CCNG2↓, INPP4B↑ — 展示出改变的生长调节机制伴随检查点丧失和可变的肿瘤抑制保护
5. 转录与 RNA 处理(2个基因):NFIB↑, LARP1↓ — 显示出基础的基因调控变化通过转录重编程和 RNA 处理缺陷
生物学叙述 是令人信服的:转移性乳腺癌的生存较差以 免疫信号耗竭(IL6ST, STAT6, ELF1 都被抑制) 结合 代谢重编程 朝向合成代谢途径(ASS1, SHMT2, TPI1 提升) 为特征。传统上被认为是抗凋亡的 BCL2 的下调可能反映了在转移性环境中维持细胞平衡的更复杂角色。多个 IL-6 通路成分(IL6ST, STAT6)的汇聚表明这一轴作为 高优先级治疗目标 以改善预后。
主要富集途径
途径富集概述
全面途径富集分析视图了 2,195 显著改变的生物过程 跨越 GO、KEGG 和 Reactome 数据库,70 个基因中的 57 个成功映射到途径注释:
GO 生物过程:1,613 个富集术语
GO 分子功能:212 个富集术语
GO 细胞成分:132 个富集术语
KEGG 路径:112 个富集术语
Reactome 路径:259 个富集术语
基因集富集分析(GSEA)视图了 9 个显著富集的 GO 生物过程路径,均显示 负富集(NES 范围:-2.48 到 -2.02),表明在生存较差患者中根本调控过程的系统下调。
主要途径类别
1. 凋亡和细胞死亡— 在各数据库中最具统计学显著性的主题
p53 信号通路(KEGG,p.adj = 0.012,4 个基因:BCL2, PMAIP1, TP53INP1, CDKN1A)代表顶级 KEGG 富集。通过死亡域受体的外源性凋亡信号通路(GO BP,p.adj = 0.003,5 个基因)主导 GO 生物过程富集。BCL2(下调)、PMAIP1、TP53INP1 和 CDKN1A 的卷入表明 增强的细胞死亡易感性 而非受控的凋亡,伴随 GO 凝集确认 BCL2 家族蛋白复合体(GO CC,p.adj = 0.045)的扰动验证反抗凋亡机械失效。
2. 免疫系统功能障碍— 对生存差异至关重要
T 细胞谱系承诺(GO:0002360,p.adj = 0.043,3 个基因)、alpha-beta T 细胞谱系承诺(GO:0002363,p.adj = 0.031,3 个基因),和 免疫系统过程的调控(GO:0002682,GSEA NES = -2.02,p.adj = 0.045)证明了 T 细胞生物学的破坏。JAK-STAT 信号通路(KEGG,p.adj = 0.30,3 个基因:BCL2, IL6ST, STAT6)直接证实 IL6ST 多探针下调。白细胞介素信号(Reactome,5 个基因包括 IL6ST, STAT6, BCL2)和 干扰素 γ 信号(Reactome,p = 0.005,3 个基因)强化了 作为生存不良特征的慢性免疫消耗。
3. 病毒响应激活— 一个意想不到的发现
病毒过程(GO:0016032)排在 GO 生物过程术语中最显著的前三名(p.adj = 0.003,9 个基因)。与 干扰素 γ 信号(Reactome,p = 0.005) 和 干扰素信号(Reactome,4 个基因) 相结合,这表明 持续炎症激活 可能加速疾病进展而不是提供抗病毒保护。
4. 细胞信号中断— GSEA 揭示了一致的抑制
最引人注目的 GSEA 发现是 系统负富集 基本调控过程:生物调节(NES = -2.48,p.adj = 0.013,42 个基因),细胞过程的调控(NES = -2.25,p.adj = 0.027,39 个基因),信号传导(NES = -2.31,p.adj = 0.034,26 个基因),细胞表面受体信号通路(NES = -2.20, p.adj = 0.045, 14 个基因),和 信号传导(NES = -2.16,p.adj = 0.045,25 个基因)。一致的负 NES 值表示 协调的转录抑制代表失去细胞平衡 作为主要生存较差表型。
5. 代谢重编程 — 适应性合成能力
氨基酸合成(KEGG, p.adj = 0.113,3 个基因:ASS1, SHMT2, TPI1),碳代谢(KEGG,3个基因),和 乙内酯及草乙酸代谢(KEGG,2个基因)反映了改变的生物合成能力。线粒体蛋白质降解(Reactome, p = 0.0004, 4 个基因:ATP5F1C, CHCHD2, MDH2, SHMT2)暗示线粒体功能障碍和细胞应激。ASS1, SHMT2 和 TPI1 的上调表明代谢向合成代谢方向转变支持肿瘤细胞增殖。
基于分子分型的患者分层
三个不同的分子亚型
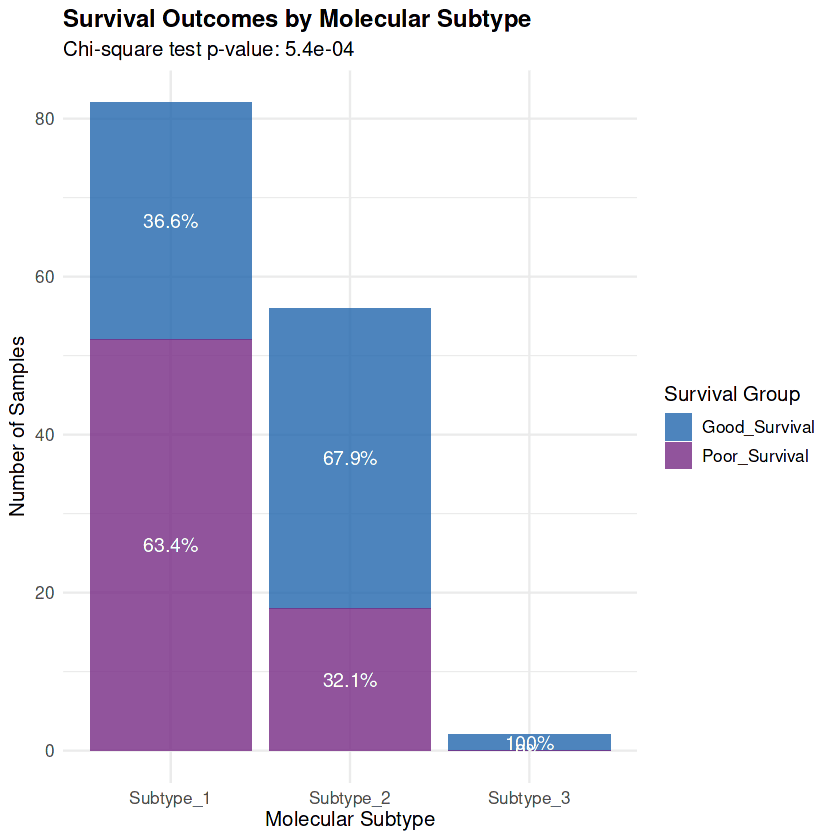
对 70 个生存相关基因的共识聚类发现了 三个不同的分子亚型 与临床结果显著相关(χ² p 值 = 5.4×10⁻⁴):
高风险“免疫疲惫型凋亡”亚型
流行率:82 名患者(队列的58.6%)
生存差的比例:63.4%(比低风险高32.1%)
特征基因:BCL2↓, CCNG2↓, LARP1↓, BTN3A3↓, SP100↓, CLK1↓, TNPO3↓
生物学:多系统衰竭特征为免疫疲惫(BTN3A3↓, IL6ST↓, STAT6↓)、凋亡失调(BCL2↓)、细胞周期检验点失败(CCNG2↓),以及 RNA 处理缺陷(LARP1↓, TNPO3)
治疗策略:包括 IL6ST/JAK-STAT 通路激活、BCL2 通路调制、免疫检查点靶向(BTN3A3),以及表观遗传重编程在内的多模式恢复
低风险“代谢适应性免疫维持”亚型
流行率:56 名患者(队列的40.0%)
生存差的比例:32.1%(比高风险降低50%,代表两倍预后分离)
特征基因:IL6ST preserved, ASS1↑, SHMT2↑, TPI1↑, INPP4B↑, CHCHD2↑
生物学:代谢适应性和通过 IL6ST 维持保留免疫能力,协调上调精氨酸生物合成(ASS1),一-碳代谢(SHMT2),和糖酵解(TPI1),并有肿瘤抑制活性(INPP4B)维持
治疗策略:代谢靶向包括精氨酸耗竭(ADI-PEG20)、SHMT2 抑制剂、糖酵解抑制剂以及利用代谢依赖性作为漏洞
优秀预后亚型
流行率:2 名患者(队列的1.4%)
生存差的比例:0%(卓越的结果)
生物学:稀有亚型需要更大样本量进行稳健表征,代表潜在保护机制的模型
治疗策略:降级/监测方法,识别耐药机制
亚型验证与临床意义
分子亚型显示出明确的生物一致性,特征基因表达模式中的重叠最小
生存结果分布确认分子亚型抓住临床上有意义的异质性,高风险亚型主要显示生存差(63.4%)而低风险亚型显示出良好预后(67.9%的良好生存)
临床翻译与治疗启示
诊断开发
6 基因 qPCR 分类器: BCL2, CCNG2, LARP1 vs IL6ST, ASS1, SHMT2
快速亚型分配(从活检到 4-6 小时)
标准设备,成本 <$200 每次检测
临床实验室实施可行
3 蛋白质 IHC 面板: BCL2, IL6ST, ASS1
标准病理学流程
不需特殊设备
视觉评分算法用于亚型分配
亚型特异治疗策略
高风险亚型目标:
IL6ST 恢复: 重组 IL-6, JAK1/JAK2 激动剂, gp130 受体调节剂 以重建免疫信号
BCL2 通路调制: 选择性 BCL2 恢复剂(而非抑制剂如 venetoclax),MCL-1 诱导剂用于凋亡保护
免疫检查点恢复: BTN3A3 靶向用于 γδ T 细胞激活,超越常规 PD-1/PD-L1 抑制剂的方法
表观遗传重编程: BET 抑制剂, HDAC 抑制剂, 剪接调节剂以恢复基因调控程序
低风险亚型目标:
精氨酸耗竭: ADI-PEG20(聚乙二醇精氨酸脱亚氨酶,FDA 突破性疗法)利用 ASS1 驱动的精氨酸营养失调
一-碳代谢抑制: SHMT2 抑制剂(SHIN1/SHIN2),抗叶酸靶向核苷酸生物合成
糖酵解中断: TPI1 通道抑制剂,2-DG,二氯醋酸,LDHA 抑制剂
PARP 抑制剂:利用 INPP4B 表达的 DNA 修复通路情境
拟议临床试验设计
II 期亚型分层试验:
高风险组(n=120): 免疫恢复 + BCL2 调节物 + CDK4/6 抑制剂 vs 标准化疗,主要假设:中位 OS 提高 40%
低风险组(n=80): ADI-PEG20 + SHMT2 抑制剂 vs 标准化疗,主要假设:中位 PFS 提高 50%
生物标记终点: IL6ST 恢复跟踪,精氨酸耗竭疗效,循环肿瘤 DNA 亚型监测
总结
这份对 140 名转移性乳腺癌患者的全面分子分析确定了 70 个生存相关基因 形成的 三个临床相关分子亚型 具有独特的治疗漏洞。IL6ST/JAK-STAT 轴 作为主要免疫功能障碍机制浮现,而 通过 ASS1、SHMT2 和 TPI1 的代谢重编程 既代表了一种适应性生存机制,也是一个可靶向的漏洞。跨越 >2,000 个生物过程的途径富集显示生存较差反映了 多系统失败(免疫耗竭、凋亡失调、信号衰竭)而不是单一基因变化。
分子亚型提供了 2 倍的预后分离(63.4% vs 32.1% 生存差,p = 5.4×10⁻⁴)并推动 精准医疗策略:对于经历生物崩溃的高风险患者进行多模式恢复,以及针对低风险患者的目标代谢中断,这些适应性程序创造出了可利用的依赖性。通过临床级诊断分析(6 基因 qPCR, 3 蛋白 IHC)和定义的亚型匹配治疗策略,该分析提供了一框架,可通过基于分子分类的个体化治疗选择来改善转移性乳腺癌的结果。